Черноуцан А. І. Про льодовиках, скороварках і теоремі Карно // Квант. - 1991. - № 3. - С. 39,42-44.
За спеціальною домовленістю з редколегією та редакцією журналу "Квант"
Якщо запитати у школяра, чому в морозний день ковзани добре ковзають по льоду, то швидше за все можна почути простий і очевидний відповідь: «Коник треться об лід, між ними утворюється тонка водяна мастило, вона і забезпечує ковзання». Однак школяреві, більш досвідченому в фізиці, така відповідь здасться занадто простим і тому нецікавим. «Ні, - скаже він, - справа тут не в терті, а в тиску коника на лід. При підвищенні тиску температура плавлення льоду стає менше 0 ° С, а лід під коником тане. »Що ж, в принципі і така відповідь має право на існування - температура плавлення льоду дійсно знижується при збільшенні зовнішнього тиску. Але фізика - наука кількісна, і тому, щоб з'ясувати, чи має це фізичне явище якесь відношення до катання на ковзанах, необхідно зробити чисельні оцінки.
Перш за все обговоримо, що таке температура плавлення (або точка танення) льоду, чим вона цікава. Як відомо, при досягненні цієї температури лід перестає нагріватися, і поглинається їм тепло цілком йде на танення льоду. Якщо ж тепло перестане надходити, що залишився лід і вода будуть знаходитися в тепловій рівновазі. Таким чином, температура плавлення - це температура рівноваги між водою і льодом при даному тиску. Так, при тиску 1 атм вона дорівнює 0 ° С. А на скільки зміниться ця температура при збільшенні тиску до 1,01 атм?
Виявляється, розрахувати зміщення точки плавлення льоду нам допоможе ... теорема Карно. Так, так, та сама теорема, в якій йдеться про максимальне ККД теплових машин. «До чого ж тут точка плавлення льоду?» - запитаєте ви. Справа в тому, що Карно довів теорему про максимальний ККД циклічної теплової машини будь-якого типу, незалежно від того, що в неї закладено в якості робочого тіла: ідеальний газ, що тане лід або мильна плівка. Необхідно дотримати лише одна умова: машина повинна отримувати тепло тільки при температурі T 1, а віддавати - тільки при температурі T 2 (на проміжних етапах теплообмін не повинен відбуватися). Максимальний ККД такої машини (її називають ідеальною машиною Карно) реалізується при повільному, оборотному режимі її роботи і, незалежно від робочої речовини машини, дорівнює
\ (~ \ Eta = \ frac {A} {Q_1} = \ frac {T_1 - T_2} {T_1} \), (1)
де А - робота машини за цикл, Q 1 - кількість теплоти, отримане машиною від нагрівача.
Мал. 1
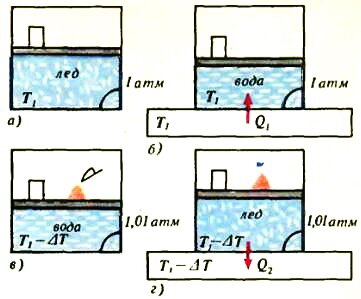
Давайте представимо нашу уявну машину Карно у вигляді циліндра з поршнем (рис. 1, а). Закладемо в неї лід масою m під тиском p 1 = 1 атм при температурі t 1 = 0 ° C (T 1 = 273 К). Постійний тиск будемо забезпечувати вантажем, що лежить на поршні. Щоб підкреслити, що вода і лід знаходяться в рівновазі, в куточку судини ми зобразили невелику кількість води.
Опишемо по етапах, як буде відбуватися один цикл в нашій машині Карно.
Мал. 2
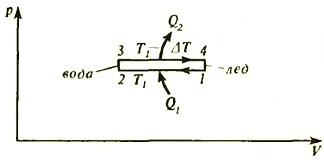
- Поставимо циліндр на нагрівач (термостат), що має температуру T 1, і передамо системі кількість теплоти Q 1 = λm, необхідне для плавлення всього льоду (λ - питома теплота плавлення). При цьому поршень з вантажем трохи опуститься (рис. 1, б), так як обсяг льоду \ (~ V_l = \ frac {m} {\ rho_l} \) більше, ніж обсяг води \ (~ V_v = \ frac {m} {\ rho_v} \). На графіку в координатах р, V (рис. 2) цього процесу відповідає лінія 1-2.
- Знімемо посудину з термостата і теплоізоліруем його (рис. 1, в), після чого будемо повільно збільшувати тиск до тих пір, поки воно не стане рівним p 1 + Δ p = 1,01 атм (для цього будемо потихеньку підсипати на поршень пісочок) . При цьому температура системи знизиться до значення T 2 = T 1 - Δ T, рівного температурі плавлення льоду при тиску 1,01 атм.
- Поставимо посудину на термостат з температурою T 2 і будемо відбирати тепло до тих пір, поки вся вода знову НЕ замерзне (рис. 1, г). На графіку (див. Рис. 2) цього процесу відповідає лінія 3-4.
- Залишилося тільки теплоизолировать посудину і повільно зняти з поршня весь пісок - і ми повернемося до початкового стану.
Тепер проведемо розрахунки. Роботу за цикл легко знайти з графіка в координатах р, V - вона дорівнює площі фігури, обмеженої графіком:
\ (~ A = \ Delta p (V_l - V_v) = \ Delta p \ left (\ frac {m} {\ rho_l} - \ frac {m} {\ rho_v} \ right) \).
Кількість теплоти, отримана від нагрівача, так само
\ (~ Q_1 = \ lambda m \).
Тому з теореми Карно (1) отримуємо
\ (~ \ Frac {\ Delta p \ left (\ frac {m} {\ rho_l} - \ frac {m} {\ rho_v} \ right)} {\ lambda m} = \ frac {\ Delta T} {T_1 } \),
або, для будь-якої температури T 1 = Т,
\ (~ \ Delta T = \ Delta p \ frac {T} {\ lambda} \ left (\ frac {1} {\ rho_l} - \ frac {1} {\ rho_v} \ right) \). (2)
Це співвідношення називають рівнянням Клапейрона - Клаузіуса. Підставивши в нього чисельні значення, отримаємо, що при Δ p = 0,01 атм Δ T = 9,2 · 10-5 К. Видно, що ефект дуже слабкий. Для зміни температури плавлення на 1 К, наприклад, доведеться створити тиск ≈ 133 атм. Повернемося, однак, до наших ковзанах.
Тиск людини в ковзанах можна оцінити як \ (~ p = \ frac {mg} {S} \) ≈ 600 Н / 2 см2 = 30 атм. Тоді зміщення точки плавлення під ковзанами складе «0,3 К, що, звичайно, дуже мало в морозний день. Так що прав виявився «наївний» школяр: мастило утворюється в першу чергу за рахунок тертя. А яка ж у такому випадку роль ковзанів? Адже вони все-таки потрібні! Чи не обговорюючи докладно «фізику катання», відзначимо один очевидний факт: для змащення поверхні коника, площа якої мала, потрібно розтопити набагато менше льоду, ніж для змащення підошви черевика.
Чи зустрічаються в оточуючій нас дійсності такі тиску, при яких відбувається помітне зміщення точки плавлення льоду? Безумовно, зустрічаються. Наведемо лише один приклад - подолання перешкод сповзаючим по схилу важким льодовиком. У тому місці, де льодовик впирається в шматок скелі або камінь, створюється дуже великий тиск, і лід починає підтавати. Льодовик як би опливає камінь в своєму русі, пропускаючи його крізь себе. Після «зняття» тиску вода на льодовику знову замерзає.
«Це, звичайно, цікаво, але вже дуже екзотично, - скажете ви.- Невже це все, чого ми досягли?» Ні, звичайно. Подивимося уважно на наш результат. Ми навчилися обчислювати, як змінюється температура рівноваги двох фаз - рідина (вода) і тверде тіло (лід) - при зміні зовнішнього тиску. Саме чудове те, що замість цих фаз можна взяти будь-які інші, аби вони знаходилися в тепловій рівновазі один з одним. Наприклад, рідина - пар, метал - розплав, тверде тіло - пар і т. Д. Іншими словами, рівняння Клапейрона - Клаузіуса справедливо не тільки для плавлення, але і для будь-якого іншого процесу переходу речовини з однієї фази в іншу (випаровування, сублімація і пр.). У формулу (2) тоді увійдуть щільності речовини в цих фазах і відповідна питома теплота фазового перетворення.
Як приклад розглянемо перехід вода - пар.
Як ви знаєте, пара, що знаходиться в рівновазі з водою, називають насиченим. Залежність між температурою насиченої пари і його тиском використовується для розрахунку вологості повітря, визначення точки роси і т. Д. Крім усього іншого, температура насиченої пари (температура рівноваги вода - пар) визначає точку кипіння води при даному зовнішньому тиску. Так, при тиску 1 атм температура кипіння дорівнює 100 С (373 К). З іншого боку, добре відомо, що тиск насиченої пари зростає при збільшенні температури. На цій властивості - зростанні температури кипіння з тиском заснований, зокрема, принцип роботи скороварки, де продукти готуються при більшому тиску і більшій температурі.

Мал. 3
У чому ж відмінність між процесами танення льоду і випаровування води? Чому в одному випадку температура рівноваги фаз з ростом тиску зменшується, а в іншому збільшується? Справа ось у чому. Коли лід поглинає тепло і плавиться, обсяг системи зменшується (щільність води більше щільності льоду), а коли вода поглинає тепло і випаровується, обсяг системи збільшується (щільність насиченого пара менше щільності води). Однак графік циклу в координатах р, V і в тому, і в іншому випадку повинен йти за годинниковою стрілкою - інакше робота машини за цикл буде негативною. Порівняйте хід обох графіків (див. Рис. 2 і 3) і ви зрозумієте, чому в одному випадку більшого тиску відповідає менша температура, а в іншому - навпаки. Спробуйте, крім того, продумати послідовність дій, які треба зробити з посудиною, що містить воду і пар, щоб вийшов зображений на графіку цикл Карно.
Ми ж завершимо нашу розповідь чисельної оцінкою зміщення точки кипіння при збільшенні тиску від 1 атм до 1,01 атм. Для цього у формулі (2) замінимо питому теплоту плавлення льоду на питому теплоту пароутворення води r, а щільність льоду - на щільність насиченого пара ρ p:
\ (~ \ Delta T = \ Delta p \ frac {T} {r} \ left (\ frac {1} {\ rho_p} - \ frac {1} {\ rho_v} \ right) \).
Щільність водяної пари при Т = 373 К і р = 1 атм знайдемо з рівняння Менделєєва - Клапейрона:
\ (~ \ Rho_p = \ frac {pM} {RT} \) ≈ 0,58 кг / м3.
Підставляючи чисельні значення, для Δ p = 0,01 атм отримуємо Δ T ≈ 0,28 К. Як бачите, в цьому випадку ефект досить помітний: щоб збільшити температуру кипіння на 1 К, треба підняти тиск всього на 0,035 атм, що цілком реально навіть при звичайних умовах.
А на скільки зміниться ця температура при збільшенні тиску до 1,01 атм?«До чого ж тут точка плавлення льоду?
А яка ж у такому випадку роль ковзанів?
Чи зустрічаються в оточуючій нас дійсності такі тиску, при яких відбувається помітне зміщення точки плавлення льоду?
Невже це все, чого ми досягли?
У чому ж відмінність між процесами танення льоду і випаровування води?
Чому в одному випадку температура рівноваги фаз з ростом тиску зменшується, а в іншому збільшується?
